Energetické zlúčeniny aminokyselín 2.
Je to zaujímavé, keďže látka kompletne rozpustená ani preplachovaná nebola, takže v liehu, pri zohrievaní, aj keď sa všetok hmoty nerozpustil, musela nastať reakcia/rozklad a tak látka bola. ako sa zdá extrémne, zbavená svojich predchádzajúcich vlastností - amorfnosť, hygroskopičnosť, tekutosť. V pôvodnej látke mohol byť a pravdepodobne aj bol nadbytok niektorého z prekurzorov, s najväčšou pravdepodobnosťou chloristanu DAA. Digitálne váhy ktoré používame majú udanú presnosť 10 mg, v skutočnosti až takmer 50 mg, podľa teploty a vlhkosti okolia). A oxid meďnatý je pravdepodobne menej koncentrovaný, ako sme predpokladali. Je to stále veľmi zaujímavé, ak by predchádzajúce výrazné vlastnosti spôsoboval len mierny nadbytok/nedostatok prekurzoru (pri experimentoch väčšinou pracujeme s dávkami 1/100 alebo 1/200 mólu). Alebo v liehu už nastal taký rozklad, že ten mrvivý prášok sa zložením už dosť odlišuje od Cu(DAA)ClO4.xH2O. Možno bola liehom vyplavená časť chloristanu meďnatého a získaná látka sa viac blíži zložením k Cu(DAA)2.
Na rade sú ešte energetické testy toho prášku. Prášok bol aj pokusne ponechaný vo vlhkom prostredí a po dvoch dňoch sa zmenil na veľmi tvárnu hmotu, pripomínajúcu plastelínu, čo by mohlo byť taktiež veľmi využiteľné (zaujímavá, značne brizantná by mohla byť "plastelína" na báze iónovej živice kov-GLY-chloristan-voda plus disperzný hliník). Po prenesení do suchšieho prostredia sa mäkká hmota po pár hodinách opäť zmenila na veľmi suchú, ľahko drobivú formu. Tá v ohni energicky deflagruje (teda obsahuje dosť chloristanu), no ani zďaleka nie tak, ako Cu GLY-chloristan (deflagrácia jeho veľkých tmavomodrých kryštálov už len tým hlukom vzbudzuje rešpekt). Hrudka zabalená v pár vrstvách hliníkovej fólie v plameni exploduje alebo skôr hlasno praskne, pričom hliníková fólia je roztrhaná len na veľké kúsky. Cu GLY-chloristan pri takom istom pokuse detonuje plnou silou a fólia je rozprášená. Po týchto pokusoch s Cu DAA-chloristanom aspoň vidno, aké rozdielne môžu mať vlastnosti podvojné soli obsahujúce rozdielne aminokyseliny. Podobné testy sa spravia aj s dusičnanom DAA a oxidom meďnatým - čo sa týka DAA ako aniónu, budeme sa koncentrovať už len na túto podvojnú soľ, prípadne, ak pribudnú pozitívne informácie, aj na ďalšie podobné obsahujúce iný bežný prechodný prvok, napr. zinok.
"Iónová živica" CuDAANO3.xH2O bola pripravená podobne ako predchádzajúci chloristan. Najprv sme v plastovej miske za horúca rozpustili CuO v roztoku dusičnanu DAA. Vznikol tmavomodrý roztok, v ktorom o malú chvíľu začali vznikať hrudky Cu(DAA)2 (mal by to byť dihydrát) a tie sa prakticky exponenciálne rozrastajú až sa rýchlo vyzráža takmer všetka soľ (je veľmi nerozpustná). Obsah misky sme vyklopili do sklenej misy, kde rýchlo po vychladnutí vytvrdol. Pre malé množstvo použitej vody vykryštalizovala aj väčšina dusičnanu Cu hexahydrátu. Na obrázkoch nižšie je ztuhnutá zmes v mise, pokus vypláchnuť plastovú nádobku malým množstvom vody, ktoré nevyvolalo takmer žiadne rozpúšťanie nalepeného zbytku a taktiež hmota v mise po priliatí vody s oškriabaným zbytkom z plastovej misky, tá voda za studena rozpustila len časť dusičnanu Cu nalepeného na modrej hmote, pričom rýchlo badať zmenu jej farby:



Potom bola misa zohrievaná na vriacom vodnom kúpeli. Na ďalších dvoch obrázkoch je vzhľad obsahu misy po 10-tich a 30-tich minútach ohrevu:


Prakticky až po jednej hodine ohrevu vznikol číry, nádherný tmavomodrý roztok alebo skôr tavenina:

Keď už bola kvapalina číra, mala sirupovitú konzistenciu. Prerušili sme ohrievanie, chceli sme vidieť, ako sa látka bez dodatočného ohrievania (v prípade niektorých DAA-chloristanov ohrev prebiehal až do stavu silného tuhnutia látok) po ochladení bude správať po dobu niekoľkých dní. Vychladnutá hmota mala potom konzistenciu ako med alebo epoxidová živica. Na povrchu sa vytvorila akási blana a v hmote v určitej vrstve a na niektorých miestach sa vyzrážalo nepatrné množstvo akoby prášku. Možno je to Cu(DAA)2 ktorý nestihol zreagovať, keďže sme hmotu zohrievali do prvých náznakov čírosti alebo nám pri manipulácii s vlhkou misou do hmoty prekĺzla kvapka vody a tá vyzrážala tú soľ. No prv sme si mysleli, že je to "všľahaný" vzduch, bublinky, od prílišného miešania taveniny a to nám dalo nápad, že v prípade takýchto hustnúcich a tvrdnúcich tavenín a zmesí s nimi by sa dala rovnomerným, ešte za horúca vmiešaním malých bubliniek vzduchu ladiť ich citlivosť a/alebo brizancia. Na obrázku nižšie je vychladnutá tavenina, ktorú ponecháme stáť niekoľko dní a potom ju opäť budeme taviť až do tuhnutia (s najväčšou pravdepodobnosťou sme látku zohrievali krátko, no aspoň uvidíme rozdiel):

Tá blana z povrchu hmoty zmizla už v prvý deň a po troch dňoch bola látka očividne viskóznejšia a rovnako číra, keď nepočítame to malé množstvo zrazeniny. Je zaujímavé, že tieto látky nie sú hygroskopické do stavu úplného, stabilného roztečenia sa a nerozložia sa státím na vlhkom vzduchu. Na obr. nižšie je látka už konzistencie tuhnúcej epoxidovej živice:

Ryhy urobené v látke pri takejto viskozite sa ako-tak zahladia až po cca hodine. Troška odobranej vzorky pri kontakte s vodou reaguje typicky - veľmi rýchlo sa rozpúšťa, v menšom množstve vody na tmavomodrý roztok, v závislosti od koncentrácie sa niekoľko sekúnd nič nedeje, no do pol minúty sú už zreteľné chumáče vločkovitej zrazeniny a okolo minúty roztok obsahuje hustú, objemnú zrazeninu hydratovaného Cu(DAA)2:



Živičnatá hmota bola ponechaná vo vonkajšom prostredí dva dni (počasie bolo slnečné), no vo viskozite badať nie veľmi veľkú zmenu:
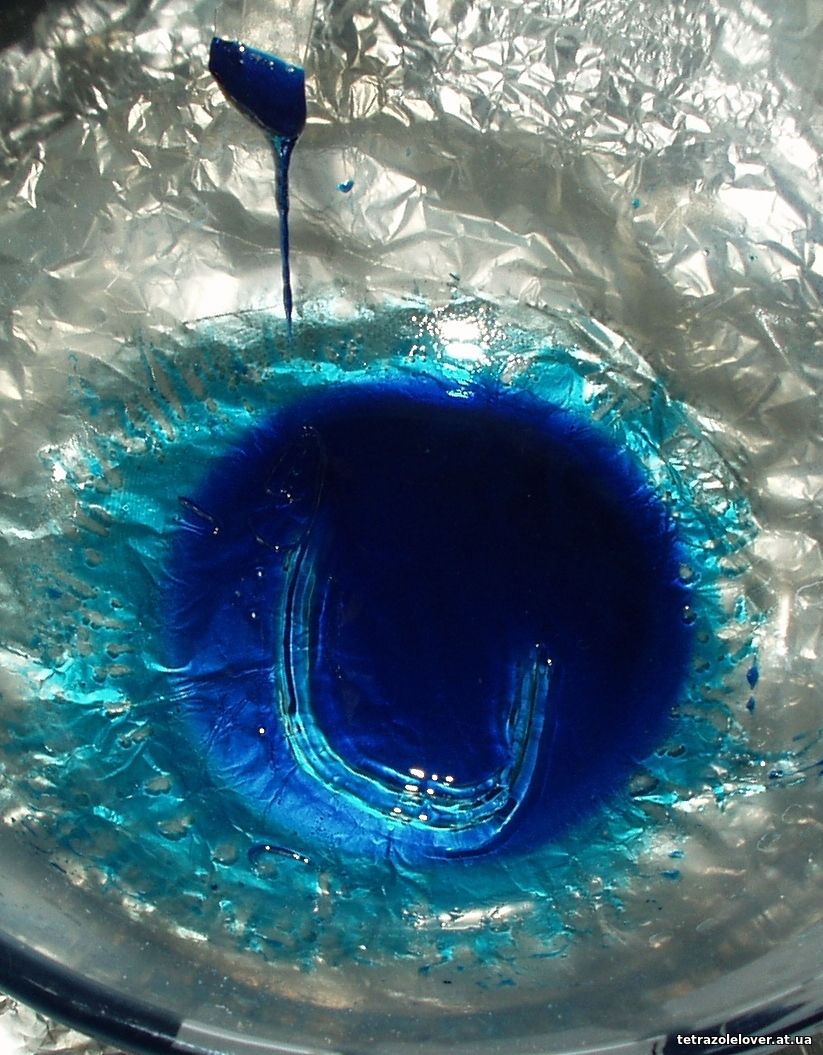
Malá vzorka CuDAANO3.xH2O bola ponechaná v kontakte s hrubokryštalickým dusičnanom amónnym, aké zmeny nastanú:

Očakávali sme, že kryštály dusičnanu sa rýchlo rozpustia a celá zmes sa roztečie na kvapalinu, no zatiaľ to vyzerá tak, že sa nič také nedeje, kryštály sú celé, modrá živica len prenikla do puklín a nerovností kryštálov. Je to veľmi dobré znamenie. Ideálne bude ešte neskôr pridať hliníkový prach a celú zmes vzduchotesne zabaliť do voľnej plastovej fólie a pozorovať, či sa bude tvoriť vodík alebo či sa bude zmes zohrievať. Po pár dňoch, ako látka pomaly pretiekla cez kryštály, keďže sme misku so zmesou mierne naklonili, bolo badať, že zbytky látky hore boli stále živičnaté, kým pretečená látka bola sirupovito-medovitá a nebolo badať na nej náznaky rozkladu, no aj tá na vzduchu časom opäť tuhne. Voda, ktorú "vysala" z kryštálov dusičnanu amónneho opäť uvoľňuje. Skvelé. Taktiež na kryštáloch nebadať veľmi výrazné zmeny. To sú skutočne vynikajúce výsledky testu, teraz o takýchto látkach debatujeme v superlatívoch. Ešte príde na rad test s hliníkom. Vzhľad zmesi po pár dňoch:

Je zaujímavé, že ani po dlhšom čase tá časť živice, ktorá neprišla priamo do kontaktu s dusičnanom amónnym neprevzala vlhkosť z kryštálov alebo už z pretečenej časti, ktorá je stále v priemere redšia a badať v nej po ochladení akoby tvorbu malých kryštálov dusičnanu, no žiadny rozklad. Teda malé množstvo dusičnanu sa v živici rozpustilo a ten zvyšuje hygroskopicitu. Ako sme spomínali vyššie, na rad prišiel test reakcie s atomizovaným hliníkovým prachom a to tak, že veľké kryštály NH4NO3 pokryté živicou sme vložili do malého sáčku a prisypali sme trochu Al prachu a zbytok živice sme s ním najprv zmiešali a až tak sme ho vložili do toho istého sáčku tak, aby sa steny sáčku k sebe zlepili (pred jeho uzavretím sme z neho opatrne vytlačili čím viac vzduchu). Tak bude možné lepšie sledovať možnú tvorbu bubliniek v zmesi a zmenu jej farby. Všetko bolo potom voľne zabalené do pár vrstiev hliníkovej fólie, aby prípadné vznikajúce teplo pôsobilo katalyticky. Vzhľad zmesi v sáčku:

Na zbytku zmesi s hliníkom v naklonenej miske po pár dňoch badať, že sa zložky pomaly od seba oddeľujú (vzorky budú kontrolované vždy po pár týždňoch, prítomnosť aminokyseliny má nepochybne stabilizujúci účinok):

A po pár týždňoch (hliník sa zdá byť nezmenený):

A taktiež v sáčku po pár týždňoch farebné zmeny alebo tvorba plynov negatívne:

Zbytok látky bol opäť zohrievaný na vodnom kúpeli, či sa vytvorí sklo. Po takmer dvoch hodinách zohrievania bola hmota stále veľmi poddajná, plus nastali očividné zmeny - povrch látky zmenil farbu, vyzrážala sa svetlá látka a vytvorili sa v ňom bubliny:

Pod bledou bublinatou vrstvou je hmota, zdá sa, stále číra. Taktiež na hmote už predtým nalepenej na stenách misy nebadať nejakú výraznú zmenu. Látka sa buď zohrievaním už na vodnom kúpeli rozkladá alebo obsahovala nadbytok niektorého prekurzoru, ale možno aj vodná para víriaca okolo misy mohla toto spôsobiť, no to je málo pravdepodobné. Hmota po vychladnutí už bola sklená, teda aspoň povrch a nalepená na stenách, hlbšie vrstvy boli aspoň niekde veľmi húževnaté, tam by nebolo možné hmotu dezintegrovať:

Jemný svetlý prach vytvorený na povrchu hmoty tĺčikom na vzduchu rýchlo tmavne. Hmotu necháme stáť niekoľko dní a ak sa zas zmení na použiteľnú živičnatú hmotu, vyskúšame jej rozpustnosť v acetóne alebo liehu a tiež ju vyskúšame skombinovať s NH4NO3 (pozri vyššie), hliníkom alebo aj s tritolom a otestujeme detonovateľnosť a prípadne aj brizantnosť kompozície. Aj po pár dňoch sa látka zdá byť veľmi tvrdá, no nie krehká, asi ako zle vytvrdnutá epoxidová živica a v skutočnosti je veľmi plastická - tĺčik stojaci na povrchu látky sa za ten čas do nej vnoril, bolo ho treba pomerne veľkou silou vylomiť. Na tĺčiku nalepenej látke bolo badať veľmi vláknitú štruktúru, ktorá o určitý čas zmizla. Vzhľad hmoty po pár dňoch (ešte počkáme, ako sa bude meniť, no zdá sa, že je v stabilnom stave, aj tá tenká vrstva na stenách misy a v chladnejšom prostredí hmota krehne. Zaujímavé):

Ani po viacerých dňoch sa hmota takmer nezmenila, preto k nej bol priliaty technický etanol, či nastane rozklad alebo či sa hladko rozpustí. Niekoľko hodín nebolo badať zmeny, no potom, ako sa niečo liehu odparilo a v kvapaline stúpol obsah vody, sa začala vytvárať objemná vločkovitá zrazenina a modrý roztok, teda zdá sa, že látka v pomerne koncentrovanom alkohole rozpustná nie je - dobrá informácia, čo látku posúva na široké pole pre experimenty. Zo vzniknutej zmesi sme neskôr skúsili opäť získať pôvodnú "živicu" (no ak bude problematická, použijeme novú várku a potom tú použijeme na experimenty s plastifikáciou či so zhutňovaním zmesí) a ako sme očakávali, látka už nebola číra, aj keď sa zdá, že tá modrá zrazenina nemá tendenciu byť rovnomerne rozptýlená, ale vytvára zhluky. Tá zrazenina, nerozpustný prach, bude pravdepodobne zásaditá soľ, čo by nemalo interferovať s našimi pokusmi, keďže v zmesi je jej málo (je to zaujímavé, aké má tento CuDAA-NO3.xH2O vlastnosti, keďže dusičnan DAA sa nám nepodarilo pripraviť v tuhom stave - aj v suchom prostredí si drží tekutosť). Prvé zmesi budú testované s dusičnanom amónnym a hliníkovým prachom. Ďalšou fázou pred testami bolo pridanie jemne kryštalického dusičnanu amónneho k modrej hmote, zohrievanie a miešanie, kým nevznikne homogénna zmes. Na vytvorenie dobrej zmesi stačilo pár minút na vodnom kúpeli:


Za horúca bola zmes hustá a lepkavá, no po vychladnutí veľmi stvrdla a prilepila sa na sklo, a to sme čakali, že bude stále poddajná a ľahko sa oddelí od stien nádoby. Necháme ju stáť na vzduchu, či a ako sa zmení. Zaujímavé bolo, že po pridaní dusičnanu amónneho sa z modrej látky uvoľnil zreteľný zápach, mierne kyslastý, dráždivý, žiadny náznak čpavkového. Zmes po vychladnutí:

Zápach sa prakticky stratil už po jednom dni státia na vzduchu, taktiež za deň už pribudla vlhkosť, zmes sa opäť zmenila na mäkkú a lepkavú, čo vyžadujeme - chceme testovať zmesi husté, lisované, s minimálnym množstvom uzavretého vzduchu, niečo vzdialene porovnateľné s eutektikami organických dusičnanov s anorganickým(i) alebo so zmesou vysokoaluminizovaného amonalu s väčším množstvom vody (aj keď pri našich experimentoch používame hliníkový prach, keďže je to jeden z najlepších senzibilátorov, ale vôbec ho nepovažujeme za ideálnu prímes a do budúcnosti s ním nepočítame, pre jeho reaktivitu a ťažkosti ho pripraviť vo veľmi jemnej forme v primitívnych podmienkach, čo aj často spomíname. Hľadáme iné, lacné, dostupné a stabilné riešenia, možno aj tieto látky na báze kovu, aminokyselíny a oxidujúcej kyseliny budú vhodné aj samostatne, ale to otestujeme postupne, trpezlivo. Ale zas napríklad použitie hliníka vo forme fólie v termobarických zbraniach považujeme za ideálne). Konzistencia zmesi bola prakticky nemenná už po jednom, dvoch dní státia na vzduchu. Aj keď použitý dusičnan amónny bol zreteľne kryštalický, zmes je pomerne tvárna a veľmi lepkavá. Z obrázku nižšie sa dá dedukovať jej konzistencia:
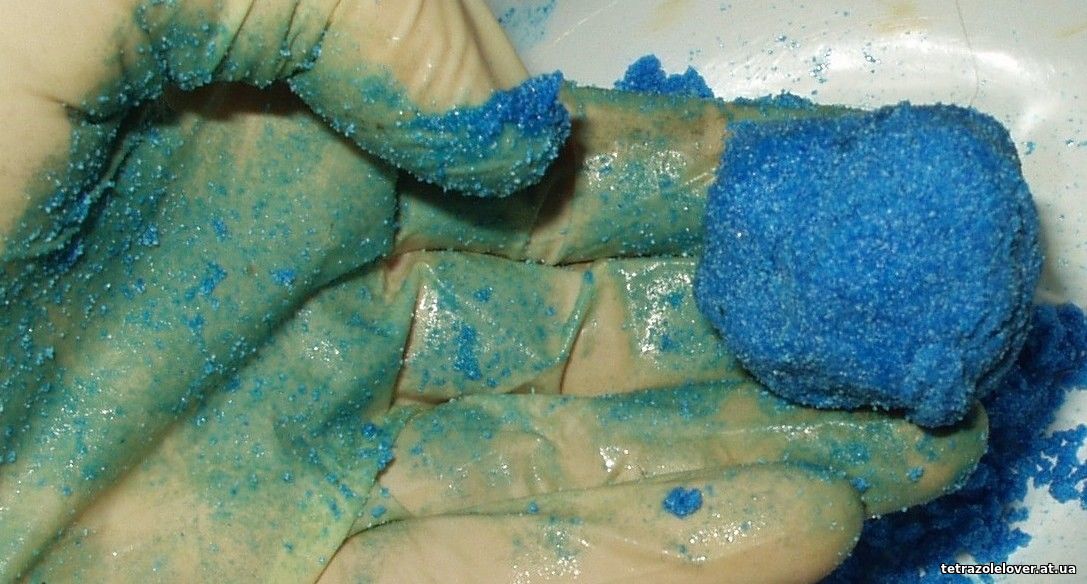
Ďalšia fáza bola rozotrenie zmesi v trecej miske na jemnú pastu. V trecej miske sa zmes rýchlo menila na veľmi lepkavú plastickú hmotu (dosť pripomínajúcu mäkšiu plastelínu), po čase v kľude získala určitú pružnosť a neskôr sa už dala ľahko deliť. Jej výzor:

Po pár dňoch sa dala opäť mrviť až na taký lepkavý prášok, vďaka rastu a zrastaniu kryštálov dusičnanu amónneho. Lisovať sa ale dá zatiaľ skvelo. Vzhľad:

Potom bol pridaný hliník (lístkový/atomizovaný 1:1, zložky v zmesi sú teraz v pomere 70/22/8 DA/CuDAANO3.xH2O/Al) a zmes bola zas dokonale premiešaná, vyhnietená. Dá sa dosť dobre mrviť, ale aj lisovať:

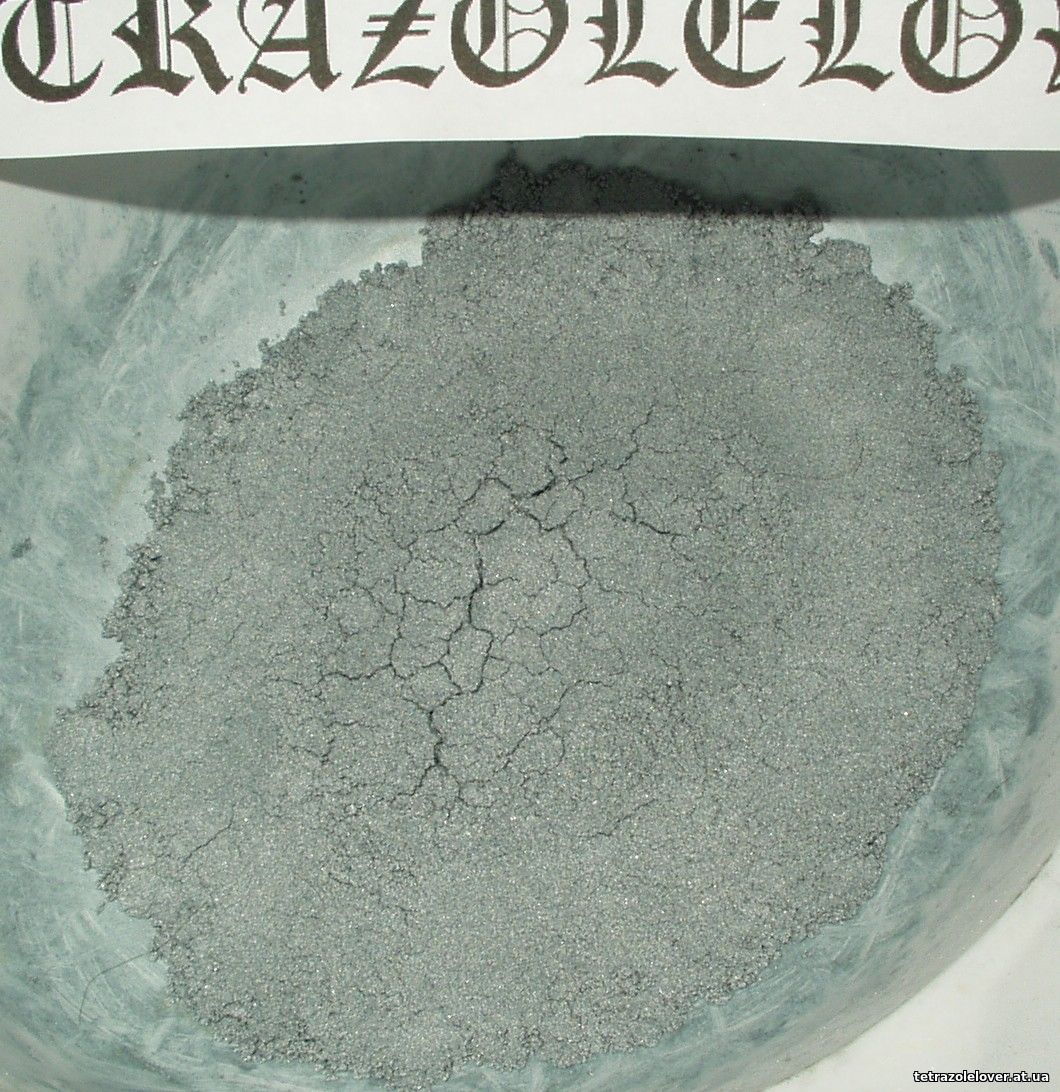
Zmes sa dá poľahky lisovať na hustotu cca 1,5 g/cm3, čo je nad kritickými hustotami bežných amonoliadkových trhavín. Ale kým sme sa zaoberali inými trhavinami a dohadovali nad metódou testovania, spomínaná zmes stihla značne stvrdnúť v nádobke, v ktorej sme merali jej hustotu. Osud chcel, aby test bol iný než sme plánovali, čo možno bude ešte zaujímavejšie. Nezdá sa, že by zmes zmenila farbu alebo stúpol jej objem:

Sa smejeme, hahaha, nad tou zmesou, keďže sme nečakali, že do nej budeme musieť vŕtať dieru. Pôvodne sme mysleli, že sa bude dať pomrviť na prášok, no hmota bola tvrdá ako kameň. Rozbušku sme použili pentolitovú, kompletná náplň aj s traskavinou cca 700 mg, Dalo sa čakať, že detonácia bude nekompletná a budú najdené zvyšky, no zvuk bol dunivý a aj v zemi bolo cítiť slabšiu vlnu, takže na začiatok nie zlé. Mali sme pripravený aj samostatný sirupovitý dusičnan DAA a premýšľali nad otestovaním v podobných zmesiach (aj nad jeho zmesami s koncentrovaným roztokom dusičnanu trietanolamínu, keďže je veľmi lacný a ľahko dostupný vo veľkom množstve, a preukazuje veľmi dobré vlastnosti v trhavinách. Hlavne vysoko zvyšuje pracovnú schopnosť, uľahčuje lisovateľnosť práškových trhavín a plastifikuje bez toho, aby výrazne znižoval citlivosť trhaviny. Veľmi úspešne sme napríklad testovali pastovité zmesi tritolu, dusičnanu sodného a roztoku dusičnanu TEA. Citlivosť na iniciáciu, kritický priemer a výkon zmesí boli prekvapujúce). No ukázalo sa, že minimálne v tekutom vlhkom stave je nestabilný: steny nádoby, aj keď tá bola celý čas otvorená, sa akoby zarosili veľmi zapáchajúcou látkou (to už bol poškodený plast), a to homogénne, aj keď kvapalina na dne nádoby nebola rozliata rovnomerne. Očividne uvoľňuje kyselinu dusičnú a kryštalická, ťažko rozpustná zrážajuúca sa látka je pôvodný DAA. Preto ho neskladovať. Chloristan by bol v podobných pomienkach neporovnateľne stabilnejší a samozrejme ten meďnatý komplex/podvojná soľ zatiaľ vykazuje excelentnú stabilitu
Okolo tu spomínaných bio-energetických materiálov sme rozprúdili debatu aj v zahraničí, uvidíme, kam to posunie vývoj v tejto oblasti (súkromná komunikácia alebo publikovanie vo vedeckých papieroch, čo už aj je).
V oblasti zlúčenín s dusičnanovým aniónom sú momentálne v strede nášho záujmu zlúčeniny obsahujúce DAA (ako anión vo vyššie spomínanej podvojnej soli a možno neskôr objavíme jeho ďalšie využitie) a kreatín (katión - z tohto sa pokúsime vyvinúť lacnú, no účinnú a citlivú kompozíciu, hlavne pre jeho hustotu a ľahkú prípravu z bežných surovín, dokonca sú tendencie použiť kompozíciu na jeho báze vo vrstvených termobarických náložiach - vo vonkajšej vrstve. Inakšie sú jeho zmesi, pokiaľ neobsahujú iný senzibilátor, napr. hliník, dosť necitlivé. Napr. na nálož zmesi DA/DK/RO 79/20/1 sa nepreniesla detonácia z 25g náložky alumatolu 90/5/5), kým pri chloristanoch je to Gly (anión/katión, ligand) a kyselina guanidínoctová (katión, ligand, pri chloristane sa ukazujú problémy s hustotou/lisovaním, uvidíme neskôr, po testoch brizancie). V poslednej dobe sme sa dosť zaoberali cyklizáciou kreatínu na kreatinín, skúšali sme rôzne metódy, najlepšou je určite použitie mikrovĺn, teda určite nie v lese, tam je to pomalé odparovanie horúceho roztoku kreatínu s nadbytkom HCl, čo tiež funguje skvele. Otestujeme teda aj kreatiníniové zlúčeniny, najviac nás zaujíma chloristan, či je dostatočne málo hygroskopický, citlivý a či má dostatočne nízky kritický priemer, aby mohol byť použitý v rozbuškách ako sekundárna náplň. Dusičnanom sa asi veľmi zaoberať nebudeme, zdá sa byť značne rozpustnejší ako dusičnan kreatínu, ktorý sa izoluje a vyrába veľmi ľahko (hoci podvojnou zámenou).
Zdá sa, že práve chloristan kyseliny guanidínoctovej (glykokyamínu) je zlúčenina majúca najlepšie vlastnosti, čo sa týka nízkej rozpustnosti a hygroskopicity (ak berieme v úvahu bežne dostupné dusíkaté organické kyseliny), vzdialene pripomína chloristan amónny. No kvôli zlej kryštalickej štruktúre má zdanlivo nízku hustotu. Zdá sa, že kryštalizuje vo forme malých platničiek. Bol testovaný zatiaľ iba v plastovej rozbuške. Skutočne ho bolo problematické vhodne lisovať. Detonoval od kombinácie 30 mg NAGP / 100 mg PETN, no zlúčenine chýbala výrazná brizancia, je treba spraviť ďalšie testy. Možno to bude v prípade potreby vhodná, alternatívna sekundárna náplň do rozbušiek, ako napr. podvojné gly-chloristany. Ako vyzerala prvá pripravená vzorka:

Potom bolo vyskúšané inú várku kryštalizovať pomaly (vzorka hore vykryštalizovala zo zohrievaného roztoku), kryštály teraz naozaj boli doštičkovité, viachranné, taktiež pripomínajúce tabulárne kryštály baritu (na fotkách to nevidieť dobre), nie je vylúčené, že nastal aj rozklad alebo cyklizácia:

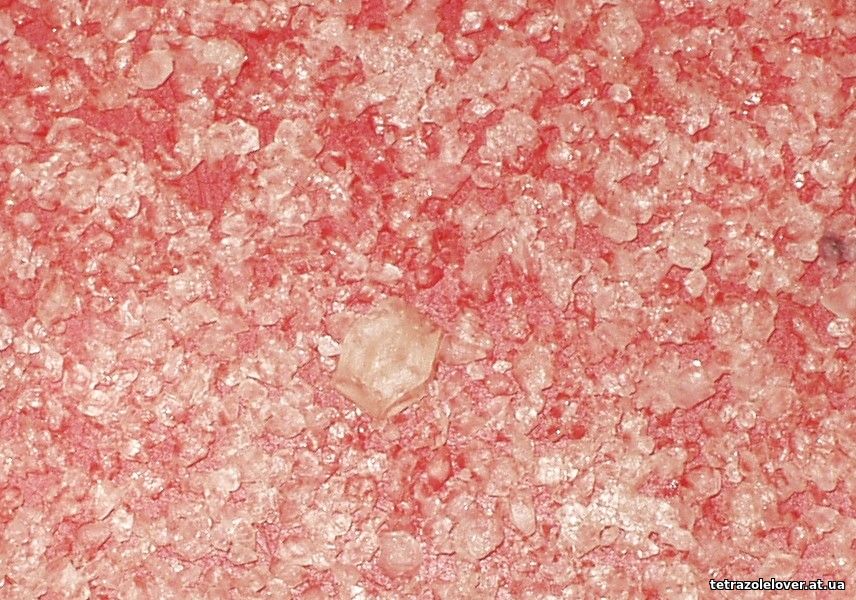
Kryštály sú mäkké, ľahko sa "pučia", pomletý chloristan má dosť zlú konzistenciu, je veľmi kyprý (pre porovnanie, obyčajný dusičnan kreatínu s troškou preháňania pripomína skôr piesok).

O glykokyamíne sa píše, že je značne odolnejší voči cyklizácii v kyslom prostredí (na glykokyamidín, 2-amino-1,5-dihydro

Glykokyamín perchlorát je pre nás miernym sklamaním, aj keď sa zdá, že sa dá ľahko iniciovať a má malý kritický priemer, ale zas nie ako ideálne trhaviny, možno to bude pár mm, no je problémom ho lisovať na vyššie hustoty a zatiaľ po zopár testoch skôr výkonovo pripomína dusičnan GLY a jeho zmesi. Pripravujeme ďalšiu várku, pri ktorej si dávame záležať, aby tam ani náhodou nebol nadbytok HClO4 a nechávame kryštalizovať v chlade. Látka kryštalizuje neuveriteľne ľahko, aj keď je dobre rozpustná vo vode - z minúty na minútu sa z kvapiek roztoku nalepených na stene nádoby formujú kryštály (opäť tie lístkovité, pripomínajúce sľudu). Teda, pokiaľ nie je zohrievaná a neobsahuje nadbytok kyseliny, nezdá sa byť vôbec hygroskopická. Zlúčeninu chceme otestovať lepšie lisovanú a v tenkých rúrkach, či sa naozaj oplatí ňou zaoberať. A taktiež nás zaujíma dlhodobá stabilita - máme vzorku zmesi chloristan glykokyamínu/ChA, 1:1, má hnedastú farbu (aróma je ale tá typická citrusová, nič dusíkaté) a pôsobí dojmom, že je vlhká (nadbytkom kyseliny to nebude, tá by za ten čas už bola dávno neutralizovaná zásaditými výparmi zo vzduchu, čpavkom alebo pyridínom, čo je u nás typické - kvapky HClO4 nalepené na nádobe alebo pipete sa zvyknú zmeniť na biely prášok v priebehu 2 týždňov), no už sa nepamätáme, ako presne sme ten konkrétny chloristan vo vzorke pripravili (asi bol zohrievaný v roztoku), no tušíme, že ak je pripravený kompletne za chladu, nebudú s ním žiadne problémy. Keď teraz porovnávame "studenú" vzorku so zohrievanou, sme trochu optimistickejší. Očividne zohrievanie zhoršuje aj mechanické vlastnosti zlúčeniny, pravdepodobne dlhým pôsobením tepla nastáva aj rozklad, nie len cyklizácia. Odporúčame preplachovať liehom (ten ale nie je ideálnou preplachovacou kvapalinou, chloristanu sa trochu po chvíli rozpustí, vyzerá to na vlhkosť ktorú technický lieh nasaje zo vzduchu, takže treba premývať a sušiť rýchlo, izopropylalkohol by mal byť ale lepší a asi aj acetón), zdá sa, že aj pri použití mierneho nadbytku glykokyamínu badať medzi kryštálmi nepatrné neschnúce stopy kvapaliny (je možné, že to spôsobuje prímes v glykokyamíne z procesu výroby, určite glycín). Nedalo nám, a ešte raz sme skúmali vplyv zohrievania na roztok glykokyamín perchlorátu, no teraz sme roztok zohrievali až kým bolo badať, že už ďalej neschne - zmenil sa na hustú kašu ktorá na stene horúcej nádoby ani v tenkej vrstve neschla. Vypli sme zohrievanie a miešali až kým látka sa postupne nezmenila na kryštalický prášok, ktorý už prekvapujúco nevykazoval náznaky vlhkosti. Z toho sme usúdili, že nastala čiastočná cyklizácia a tento nový chloristan obsahujúci imidazolové jadro je iónovou kvapalinou taviacou sa pri teplote nižšej ako 100°C. Chceli sme si to overiť, tak po vychladnutí kryštálov sme ich opäť zohrievali na vodnom kúpeli, no už márne, nedosiahli sme tekutý stav (možno kryštály boli len "lepkavejšie"), ani pozorovaním hladkého skleného povrchu nádoby, čo je skvelá metóda na zistenie prítomnosti kvapaliny, sme nenašli isté známky tavenia, možno len nepatrnými náznakmi. Je to trochu záhada, možno pri chladnutí nastáva decyklizácia, samozrejme ešte v prítomnosti malého množstva vody, ktorá sa naviaže späť na molekulu a potom už suchá látka je necitlivá na opätovné pôsobenie tepla. Ale zaujímavé je, že kryštály takto získané, teda miešaním látky až do kompletného vychladnutia/vyschnutia, majú omnoho lepšiu struktúru a prášok vyššiu hustotu ako drvené kryštály získané odparovaním za studena, čiže, ako sme skôr zistili, naozaj zohrievanie zhorší vlastnosti kryštálov, ak potom tie kryštalizujú v pokoji a za chladu z nadbytku vody, no ak je kryštalizácia vynútená za ustavičnej agitácie, kryštály majú neporovnateľne lepšie vlastnosti (nemajú samozrejme až takú hustotu, ako napr. chloristan pyridínu, no dajú sa omnoho ľahšie lisovať). To môže byť v určitom zmysle kontraproduktívne, ak pri tejto látke citlivosť klesá a kritický priemer stúpa s hustotou. Tu vidno kryštalický prášok po stuhnutí tej miešanej "taveniny":

Po nových testoch detonovateľnosti sme zistili, že tento chloristan má vlastnosti veľmi podobné tritolu, teda kritický priemer a iniciovateľnosť - látku sme v rúrkach s priemerom okolo 5-6 mm bežným množstvom chloristanu bis(aminoguanidín) niklu a oddeľovacou vrstvou z pentritu nedonútili stabilne detonovať a to bola len veľmi mierne lisovaná. Brizancia vzorky pripravenej zohrievaním bola porovnávaná s tritolom (na plechu ležmo, akú širokú dieru zanechajú), v 1,5 ml ampulkách Eppendorf, nelisovaná mala veľmi malú brizanciu, kým lisovaná bola porovnateľná s lisovaným tritolom, alebo bola o trochu menej výkonná, ale to mohla spôsobiť iná hmotnosť a hustota trhavín, testovali sme ich na objem, čo nás teraz najviac zaujíma (bola by hlúposť plniť nádoby s daným objemom rovnakým množstvom trhaviny pri rovnakej hustote, ak tam pri jednej ešte zostane prázdny priestor). Ako zisťujeme, kombinovanie s dusičnanmi vo vlhku, ako v prípade pyridín perchlorátu, je veľmi nevýhodné - už s NaNO3 nastáva podvojná zámena a tvorí sa menej rozpustný dusičnan glykokyamínu. Pre zlú kryštalickú štruktúru musí byť pred lisovaním veľmi dobre pomletý, až na púder - takto sa dá lisovať pomerne dobre (podarilo sa nám zatiaľ na takých cca 1,4 g/cm3, no to už prudko stúpa kritický priemer - karboxylová skupina v molekule veľmi neprospieva takýmto zlúčeninám, toto je spoločným nedostakom týchto bio-energetických materiálov, čo sa však malým prídavkom citlivého chloristanu, napr. pyridínu, dá napraviť), ale inak nie. Novú vzorku zrevidujeme vo videu.
Pre pomerne príbuzné energetické materiály - vyrobené z liečiv, vytvoríme nový oddiel, ako sme už spomínali.
V poslednej dobe sa nám podarilo pripraviť zaujímavé bio-trhaviny dĺhým státím zmesí, ktorých zložky zohrievaním na vodnom kúpeli reagujú veľmi pomaly, čiže hydrotermálna príprava by bola energeticky veľmi náročná. Reakcia prebehne hladko niekoľkotýždňovým státím pri izbovej teplote a dá sa okamžite spustiť alebo urýchliť pridaním malého množstva už hotovej trhaviny z predchádzajúcej várky, ktorá ale nemusí mať rovnaké zloženie. Vychádzali sme z toho, že dusičnany alebo chloristany aminokyselín a podobných zlúčenín sú často ťažko iniciovateľné, kým kovové komplexy ľahko, takže sme pripravili prechodné látky, očividne veľmi stabilné. Počítame s nimi v miniatúrnych kumulatívnych a EFP náložiach. Myslíme si, že sú bez preháňania hodné patentovania. Jednoduché dusičnany alebo chloristany aminokyselín a podobných dusíkatých látok hodnotíme ako veľmi nevýhodné kvôli ich kyslosti, preto sa zameriavame na komplexy kovov, pričom neutrálna aminokyselina môže mať ešte aj stabilizujúci účinok v prítomnosti kombinácie vody a práškových kovov. A ak katiónom sú alkalické kovy alebo amín, prídavky fosfornanov do trhavín z nich robia energetické materiály novej generácie.
Opäť sa vraciame k Cu GLY-chloristanu - skúsili sme pripraviť jeho komplex s aminoguanidínom. Pripravili sme takmer koncentrovaný roztok podvojnej soli (v o niečo väčšom množstve vody, v ktorom sa soľ kompletne rozpustila - azda okolo takých 38 ml na 1/50 mólu) do ktorej sme pridali 1/100 mólu bikarbonátu aminoguanidínu, ktorý sa prv len rozpustil za mierneho šumenia, pričom roztok zostal kráľovsky modrý, len o niečo stmavol, ale o pár minút sa začala zrážať fialová kryštalická látka (pričom roztok zostalo rovnako modrý), totožná s Cu bis(aminoguanidín) chloristanom, teda komplex s podvojnou soľou asi nevzniká. A do rána po ochladení a miernom odparení sa vyzrážala modrá, nie hustá látka, ktorá zas podľa vlastností je glycinátom meďnatým.
Neskôr sme našli tento papier Syntheses & Characterisation of Complexes of Copper (II) Glycinates, kde sa spomína aj podvojná soľ GLY-chloristanu s KClO4, čo nás do určitej miery zaujalo, hlavne opäť pre použitie ťažko rozpustnej draselnej soli, ale aj pre potenciálne použitie iného (organického) chloristanu, keďže s KClO4 soľ nemôže mať nejaké výrazné energetické vlastnosti, pre veľký nadbytok kyslíka (no určite zaujímavé by boli zmesi s niektorými silne redukčnými palivami, možno by boli použiteľné v NPE rozbuškách. Skôr by bol ale zaujímavejší kuprát s chloristanom amónnym, ak je, samozrejme, pripraviteľný). Niečo vyskúšame a neskôr pridáme (dostali sme aj skvelý nápad, ako jednoducho pripraviť určité aminokyselino-chloristanové komplexy). Pokúsili sme sa pripraviť chlorečnanovú verziu, no zdá sa, že priamou reakciou GLY-chlorečnanu a KClO3,1:1, vo vodnom roztoku a jeho následným ochladením soľ nevzniká, jednotlivé zložky kryštalizujú samostatne (skúsili sme aj veľmi pomalé odparovanie zo zriedených roztokov, kryštály vznikli už iné, no stále dvoch látok, je to tretí obrázok):



S NaClO3 sme kryštalizáciu z roztoku urýchlili jeho zohrievaním na horúcom kúpeli do formovania prvých kryštálov po cyklických ochladeniach roztoku, teda kryštály sú malé, no akoby boli všetky rovnaké, okrem malého množstva bielej látky, čo by zodpovedalo nadbytku chlorečnanu Na kvôli nepresnosti našej váhy (desiatky miligramov), plus ten gly-chlorečnan mohol byť pred vážením trochu vlhký (podvojná zámena na chlorečnan meďnatý a glycinát sodný nie je vylúčená, no to by mal byť produkt značne hygroskopický, nevyzeral tak):

Modrú látku sme opäť rozpustili vo vode a nechali pomaly odparovať. Teraz vznikli značne väčšie modré kryštály, farbou sa prakticky neodlišujúce od gly-chlorečnanu. Prítomnosť pôvodného množstva chlorečnanu sodného je ťažké badať, nevytvoril typické kryštály, skôr tam videť akoby priehľadný film ale aj nejaké rôznorodé kryštály, takže stále sme si nie istí, či nastala nejaká reakcia (asi nie, sme skeptickí):


Glycín tvorí stabilné komplexy aj s niektorými chlorečnanmi, napr. s horečnatým, pričom takisto ako aj v prípade dvojmocných alkalických chloristanov, 3 móly glycínu celkom odstránia hygroskopicitu chlorečnanu (produkt je vo vode skvele rozpustný, no absolútne nenasáva vlhkosť). Produkt sa zdá byť vysoko stabilný, ale práve pre túto stabilitu látka nemá ani zďaleka vlastnosti traskavín, čo samozrejme má aj výhody aj nevýhody. Látka sa dá samozrejme použiť ako pomerne bezpečná trhavina, no ako "traskavina" len asi v prítomnosti KClO3 a azda ešte ďalšieho paliva - látka po kontakte s plameňom deflagruje nie veľmi rýchlo a kompletne bez plameňa, je to "studený" energetický materiál.
Napadlo nám, či prípadný rozklad Cu GLY-chlorečnanu nemôže spôsobovať aj (slnečné alebo UV) svetlo. Spustili sme s ním opäť dlhodobé experimenty (niekoľkoročné), keďže sme teraz zásobení traskavinami a aj hotovými rozbuškami až-až, tak si to môžme dovoliť. Zatiaľ len fotka fluorescencie Cu GLY-chlorečnanu pod UV lampou:

Zatiaľ sa ten GLY-chlorečnan drží dobre, po niekoľkých mesiacoch na svetle a premenlivom vlhku a teplote nie sú rozoznateľné absolútne žiadne známky zmeny (ani zápach), je dobre sypký aj vo vlhku. Vyrobili sme skvelú várku, zdá sa.
Vyskúšali sme reakciu chloristanu amónneho s Cu GLY-chloristanom, v pomere 1:1. V malom množstve vody sa jednotlivé zložky rozpustili po zohriatí, no po ochladení sa už nevyzrážali, bolo treba nechať odpariť niečo vody a necháť stáť niekoľko hodín v chlade, aby sa vytvorila zrazenina. Najprv sme mysleli, že chloristan amónny reagoval, no potom sme podsvietili vyzrážanú modrú hmotu a až vtedy bolo badať bezfarebné kryštály:

Také kupráty, ako s KClO4, by mohli tvoriť s GLY-chloristanom asi len chloristany niektorých veľmi zásaditých (mono)amínov a príbuzných látok (ak ide o organické chloristany), teda napr. chloristan pyridínu nie, pyridín sa uvoľnuje už pri kontakte s inými, hoci slabými, ale neprchavými zásadami (aj s aminokyselinami). Ideálnym kandidátom na takúto zlúčeninu by bol guanidín. Hypotetický glycinátobis(chloristano)kuprát guanidínu by mal 0% kyslíkovú bilanciu, počítané s vyredukovanou meďou samozrejme - C(NH2)3[CuCH2NH2COO(ClO4)2] -> Cu+2HCl+2N2+4H2O+3CO2. Tento kuprát skúšame pripraviť reakciou chloristanu glycínu so zásaditým uhličitanom meďnatým vo vodnom roztoku, do ktorého sme pridali chloristan guanidínu (pripravený z GuHCl a HClO4). Najprv sme skúsili roztok odparovať rýchlo na vodnom kúpeli, ľahko sa tvorila homogénna modrá hmota bez nejakých "vytŕčajúcich" odlišných kryštálov. No po opätovnom rozpustení a pomalom odparovaní roztoku už bolo vidno veľké kryštály zmiešané s modrou hmotou, čiže ani tu nevznikol kuprát:

Ale to nič nemení na tom, že je to vyvážená zmes, ktorá by mohla byť skvelou náplňou do rozbušiek, hoci aj typu NPED, takže bude testovaná po opatrnom rozomletí (predpokladáme, že žiadna podvojná zámena nenastala, to by bola zmes hygroskopická, jedine, že by potom produkty tvorili spolu novú, nehygroskopickú podvojnú soľ). Zmes detonuje dobre aj pri malých priemeroch, no očividne s klesajúcim priemerom klesá aj brizancia. Zmes sme prepláchli technickým liehom, pri ktorom máme podozrenie, že asi spôsobuje rozklad podvojného gly-chloristanu - vytláča/vyplavuje chloristan meďnatý, ale je to len podozrenie. asi to spôsobujú denaturačné prísady a/alebo prítomná voda - kvalita týchto technických liehov ide každým rokom dolu, výrobky z pred pár rokov boli veľmi čistým liehom, no teraz to je zvláštna zmes, ktorá pripomína etanol čoraz menej. Na preplachovanie zlúčenín už technický lieh absolútne neodporúčame, treba použiť izopropylakohol, ten sa zdá byť zatiaľ dosť čistý (no uvidíme, ako nemilo nás tento odporný podfukársky kapitalizmus ešte (ne)prekvapí).
Jedny z najmenej rozpustných bežných meďnatých komplexov aminokyselín sú možno komplexy s arginínom. Skúsili sme reakciu roztoku hydrochloridu L-arginínu (nemáme čistý arginín) so zásaditým uhličitanom meďnatým (bol pridávaný až kým sa rozpúšťal). So šumením sa vytvorila kvapalina farby tmavej kráľovskej modrej, čo by mohol byť roztok chloridu bis(arginín) meďnatého alebo možno aj podvojná soľ arginináto-chlorid, no nie sme si istí, či sa dá takto priamo pripraviť z uhličitanu, keďže arginín je veľmi slabá kyselina. Táto kvapalina sa dala dosť zahusťovať bez tvorenia kryštálov, ale po pridaní NH4ClO4 alebo NaClO3 sa vytvorili modré zrazeniny, s chloristanom prakticky okamžite, s chlorečnanom to chvíľu trvalo (teoreticky by to mohli byť aj chlorid amónny a sodný, no podľa konzistencie a farby to s najväčšou pravdepodobnosťou neboli). Tie sa po pridaní vody postupne rozpustili, ten chlorečnanový produkt asi ľahšie. Podľa tohto papiera by to mali byť bezvodé soli alebo monohydráty. Otázne je priame využitie týchto látok (majú dosť negatívnu kyslíkovú bilanciu) alebo skôr aj ich izolácia z takejto chloridovej suspenzie, keďže preplachovanie produktu na filtri napr. liehom môže vyzrážať aj chloridy, ak sa už tie nevyzrážali spolu s komplexom z koncentrovaného roztoku (tie modré látky sa zrážajú s dobrým ziskom len zo značne koncentrovaných roztokov, kde už majú šancu sa čiastočne vylúčiť aj menej rozpustné chloridy, takže treba použiť čistý arginín). A taktiež (dlhé) zohrievanie takéhoto roztoku nie je dobré, pretože arginín vytláča v horúcom roztoku v prítomnosti amónnej soli čpavok a vzniká arginíniová soľ. Tu vidno vplyv pridania malého (objemovo, ale molárne to bolo len mierne pod teóriu) množstva chloristanu amónneho do tmavomodrého roztoku komplexného chloridu, takmer celý roztok sa po chvíľke zohrievania, aby sa hrudky chloristanu rozpustili, a ochladení zmenil na modrú hustú kašu:

Príliš veľa voľnej kvapaliny tam nezostalo, celá masa sa dá stlačiť do hrudy bez toho, aby sa roztiekla, nepochybne sa tam vyzrážalo aj veľa chloridu amónneho, látka sa ale po zohriatí veľmi ľahko rozpúšťa aj v nepatrných množstvách vody, alebo sa možno aj taví, kým rozpustnosť chloridu amónneho sa z izbovej teploty po teplotu varu vody zmení asi len dvakrát (takže čo s tým, ako katalyzátor do amónoliadkových trhavín by sa táto zmes azda dala použiť. Produkty reakcie nebudeme separovať (vyzerá to tak, že by sa komplex dal ako-tak izolovať vymrazením). Látku sme vysušili a použili v experimentálnej trhavine - hrubo pomletý dusičnan amónny bol zmiešaný s cca 5% vysušenej zmesi a s 2,5% starého rastlinného oleja, z toho bola vyformovaná 90-gramová guľová náložka, ktorá bola iniciovaná malou rozbuškou z 0,5 ml ampulky typu Eppendorf, plnenej zmesou Cu Gly-ClO4/guanidín perchlorát, 1:1 molárne, ako sekundár (rozbuška sa zdala byť dosť výkonná, s takými ešte budú samostatné testy), snažili sme sa odhadnúť konšteláciu na hranici iniciácie, trafili sme sa dobre, detonácia z vrchu nálože, zo zvislej rozbušky, prešla až na dno, kde zanechala stopu na tvrdom bukovom dreve, ale do strán bola časť trhaviny len rozhádzaná, čiže tá modrá zmes sa dá dobre využiť ako senzibilátor v optimalizovanej trhavine aj v pomerne malých množstvách. Na experimenty s čistým komplexom sa použije potom čistý arginín, no predsa sme malé množstvo tejto zmesi rozpustili vo vode a nechali pomaly kryštalizovať, aby sme videli, či zložky budú kryštalizovať separovane, a ktorá skôr, no všetky zložky kryštalizovali takmer naraz, musia mať veľmi podobnú rozpustnosť):

-----------
Viaceré dusičnany aminokyselín nie sú príliš alebo vôbec hygroskopické (alebo ak mierne sú, tak často zmes s inou hygroskopickou látkou je hygroskopickejšia než jednotlivé zložky samostatne), pričom ich výbuch neprodukuje ohromujúce množstvo tepla a sú samozrejme často veľmi necitlivé na iniciáciu, preto je niekedy pridávanie dusičnanu amónneho nie najoptimálnejšie riešenie, už len pre jeho hygroskopicitu ale aj pre jeho nízky obsah kyslíka, čo pri CO alebo CO2 vybalancovanej zmesi dosť zníži obsah dusičnanu aminokyseliny (ak ten má značne negatívnu kyslíkovú bilanciu) a teda detonačná rýchlosť zmesi už nebude ohurovať. Preto by KClO3 a KClO4 mali byť výhodnejšie senzibilátory/oxidovadlá, hlavne chlorečnan nás zaujíma viac, keďže už samotný je energetický a výbuch jeho zmesí produkuje veľké množstvo tepla a vysokú teplotu, teda už v pomerne malých množstvách by mohol veľmi zvýšiť citlivosť dusičnanu, značne zvýšiť teplo výbuchu, pričom teor. maximálna detonačná rýchlosť azda nepoklesne extrémne. Samozrejme, prímes chlorečnanu môže spôsobiť problémy s nestabilitou, keďže dusičnany aminokyselín sú značne kyslé, ale napr. v prípade navlhčenej a postupne vysušenej zmesi dusičnan kreatínu/KClO3 sa v krátkom čase nič nedialo, žiadny zápach alebo iné zmeny (čo ešte neznamená, že pri dlhodobom skladovaní vo vlhku by rozklad nenastal - do jednej vzorky zmesi sme primiešali niečo CuO, či aj suchá zmes vyvolá po čase farebnú zmenu, teda zmenu sivej farby na modrú, zelenú, fialovú a pod. plus nejaký zápach, uvidíme neskôr, po týždni zatiaľ žiadna zmena). Detonovateľnosť a brizanciu zmesi sme už pokusne testovali (CO vybalancovanú, cca 55/45 - dusičnan/chlorečnan - chceli sme v každom prípade použiť zmes s viac ako polovičným obsahom dusičnanu kreatínu. Skúšali sme už niektoré vlastnosti aj CO2 balancovanej zmesi - nie je veľmi citlivá ani na náraz, ani trenie, deflagrácia neprešla do detonácie v malých množstvách a slabých obaloch (ani v nábojnici, no odpálenej od hrdla), teda zmes s menším obsahom chlorečnanu je ešte bezpečnejšia - skúšali sme ju po malých dávkach rozotierať v trecej miske a nenastala ani jedna iniciácia). Testovali sme štyri malé náložky rôzne silno lisované s rôzne silnými rozbuškami, mali sme dve zlyhávky a dve detonácie, takže zmes nemá vlastnosti blízke traskavinám (chceli sme testy archivovať, no po prvom teste, zlyhávke, kvôli mrazivému počasiu a vetru zoomovanie na kamere zamrzlo na malú vzdialenosť (akoby sa stále prepínalo na "makro", nezávisle na nastaveniach, to sa nám už stalo aj predtým), rozchodené bolo až za tmy, to sme už natočili len jeden pekný červený záblesk. Detonovateľnosť zmesi sme potom ešte porovnali (s použitím výkonných rozbušiek) so zmesou dusičnan kreatínu/chloristan pyridínu/NaNO3, cca 55/30/15 (množstvo NaNO3 bolo len na neutralizáciu HCl), tá druhá zmes prekvapujúco nedetonovala, dusičnan kreatínu je očividne extrémne necitlivý, viac pripomína obyčajné palivo ako trhavinu. Kým pri prvom teste sme porovnávali postupne silnejšie lisované nálože bez nejakého merania hustoty zmesi, od slabého lisovania po silné, pri treťom teste sme porovnali voľne sypkú zmes s mierne lisovanými na hustotu cca 1,15-1,2 g/cm3, pretože takáto kritická hustota zvykne byť pri značne "low-endových" chlorečnanových trhavinách. Zmesi boli 3 lisované: CO balancovaná kreatín nitrát/KClO3, CO2 balancovaná, tie isté zložky a CO2 balancovaná dusičnan GLY/KClO3. Sypká zmes bola zmesou všetkých troch trhavín v pomere 1:1:1. Rozbušky boli pentritové, z papierových rúrok, podľa našich skúseností dostatočne výkonných na univerzálne použitie s trhavinami normálnej citlivosti. A keďže už máme bohaté skúsenosti v oblasti energetických materiálov, veľmi presne sme sa trafili do "hranice" - kým voľne sypká zmes, 39 gramov, detonovala skvele a výkonne, tie mierne lisované (vždy po 37 gramov v papierových obaloch, dĺžka náplne cca 50 mm) sa prakticky správali totožne: výbuchy boli pomerne slabé, na 4 mm hrubej oceľovej platni nezanechali takmer žiadnu stopu, pričom to vyzeralo tak, že všetka alebo takmer všetka náplň sa rozložila, vzniklo veľa dymu, papierové obaly boli roztrieštené na takmer prach. Teda spolu to vyzerá na zhasínajúcu detonáciu - pri použitom priemere náloží, hustote trhaviny a sile rozbušky, nie sú tieto trhaviny schopné stabilne detonovať. Je to pre nás sklamaním, keďže sme počítali s využitím týchto trhavín v malých počinových náložkách s ešte väčšou hustotou a iniciovaných priemernými, nie príliš nadrozmernými rozbuškami. Lisované dusičnany aminokyselín sú extrémne necitlivé látky a ani chlorečnany s tým očividne veľa nenarobia. Samozrejme, sypké zmesi sa dajú použiť s bežnými, menej citlivými amonoliadkovými trhavinami úspešne, ak nie je po ruke nič stabilnejšie.
Taktiež plánujeme test podobnej zmesi s dusičnanom DAA, po teste jej krátkodobej stability, taktiež CO vybalancovanú, no už teraz tušíme, že to bude mierne problematické pre očividnú nestabilitu samotného dusičnanu DAA. Už skôr sme zistili, že dlhým státím odštepuje HNO3 a teraz sme si otestovali, že odparovaním vodného roztoku dusičnanu (na urýchlenie kryštalizácie) na vriacom vodnom kúpeli okamžite nastáva rozklad - roztok rýchlo získa štipľavý zápach a vo vzduch sa začne tvoriť tá typická "hmla". Keďže kyselina asparágová obsahuje dve karboxylové skupiny a len jednu amino-, v prítomnosti ľahko prchavej kyseliny (napr. HNO3 a HCl) má očividne prednosť jej vnútorná soľ. Samozrejme, iné to bude v prítomnosti napr. H2SO4 alebo aj HClO4 pri bežných teplotách. Takže absolútne neodporúčame výrobu dusičnanov (ani chloridov, napr. na podvojnú zámenu, tam bude lepšia reakcia síranu a dusičnanu vápenatého, keď už) kyslých aminokyselín, aspoň nie pri vyššej teplote (je možné, že zohrievaním sme vyvolali aj polymerizáciu DAA) a ak ich vyrobíte, tak ich treba skladovať uzavreté, v chlade a spotrebovať v krátkom čase. A taktiež ich pre istotu nemiešať (ani dokonale suché) s ničím, čo je citlivé na kyslosť.
Skúsili sme pripraviť podvojný DAA-chlorečnan olovnatý reakciou dusičnanu olovnatého a chlorečnanu sodného s mono-sodnou soľou DAA vo vodnom roztoku (podvojný aspartáto-dusičnan Pb už je známy), zdá sa, že úspešne, vyzrážalo sa veľké množstvo bielej, ťažko rozpustnej látky, ktorá od kontaktu s plameňom deflagruje podobne ako čierny strelný prach (DAA nie je nejaké skvelé palivo, už je príliš okysličená, preto sa od tejto soli nedá očakávať, že by mala výrazné vlastnosti traskaviny), ale vo väčších množstvách je deflagrácia už dosť nepríjemne prudká, takže treba byť s ním opatrný. Skúsili sme aj reakciu s chloristanom, no tu sme nezískali energetický materiál, teda nie s podobnými alebo lepšími vlastnosťami.


