Podvojné chloristany organický-anorganický
Najprv sme pripravili perovskit chloristan piperazíndiium sodný (ktorý má vlastnosti, ktoré ho dosť približujú ku hľadanému "svätému grálu" energetických materiálov a teoretické detonačné parametre 8917 m/s, 38,2 GPa pri 2,07 g/cm3). Inšpiroval nás papier Optimizing the oxygen balance by changing the A-site cations in molecular perovskite high-energetic materials. Prvý krát sme ho ale pripravili iným spôsobom, improvizovane, z veterinárneho odčervovacieho prípravku, obsahujúceho 45% piperazín citrátu (ukrajinskej výroby), kyseliny šťaveľovej, oxidu meďnatého, kyseliny chloristej a sódy bikarbóny. A keďže citráty piperazínu sú vo vode pomerne ľahko rozpustné, museli sme prv piperazín získať vo forme dioxalátu, postupným pridávaním kyseliny šťaveľovej do horúceho miešaného roztoku odčervovacieho prípravku. No nemali sme istotu, ktorý citrát je v zmesi (zbytok je monohydrát laktózy), preto sme prv použili množstvo kyseliny šťaveľovej vzhľadom k mono-piperazín di-citrátu (s najväčšou pravdepodobnosťou v prípravku je ale tri-piperazín di-citrát, alebo piperazín monocitrát podľa stabilných, veľkých ziskov). A zistili sme, že kyselina citrónová asi interferuje so vznikom monooxalátu (ktorý by bol asi aj tak značne rozpustnejší ako dioxalát), hneď vzniká dioxalát (vo vode veľmi ťažko rozpustný), v hocakom pomere sme kyselinu šťaveľovú pridali, zisky a rozpustnosť to napovedajú. Roztok nad rýchlo sa usadzujúcou, ťažkou kryštalickou látkou bol žltý, dioxalát bolo treba dobre prepláchnuť od zbytkov kyselín a laktózy, kým voda nad usadenou soľou bola bezfarebná (prevariť s trochou vody, nechať vychladnúť, prefiltrovať a prepláchnuť studenou vodou, potom prípadne celé opakovať, my sme to spravili 2-3 krát). Nenašli sme údaje o rozpustnosti hydrogenoxalátu, no je veľmi ťažko rozpustný. Druhý dobrý spôsob získania piperazínu by bol vo forme ditartrátu. Spomína sa aj nízka rozpustnosť monofosforečnanu, skúsili sme, no na počudovanie sa z roztoku nič nevyzrážalo (kyselina citrónová asi opäť spôsobovala vznik difosforečnanu, ktorý je vo vode dobre rozpustný a ktorý samozrejme naviazal len polovicu prítomného piperazínu, a nechceli sme použiť rozpustný fosforečnan pre podvojnú zámenu, keďže sme si neboli istí zložením citrátu). S kyselinou šťaveľovou je to asi najlepšia metóda. Prv, než sa dostaneme k nášmu postupu výroby spomenutého podvojného chloristanu a popisu jeho vlastností, tu sú nejaké údaje o piperazíniových soliach, vo forme obrázkov, ktoré sme našli:
.
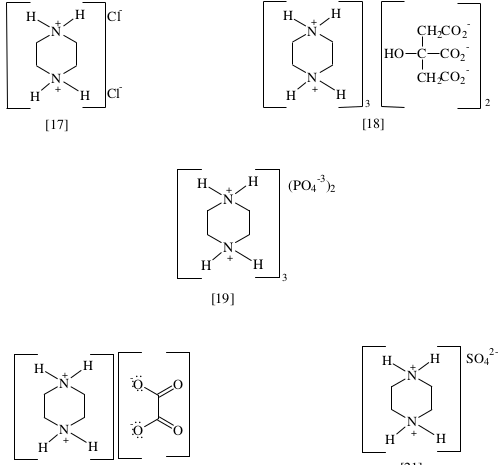

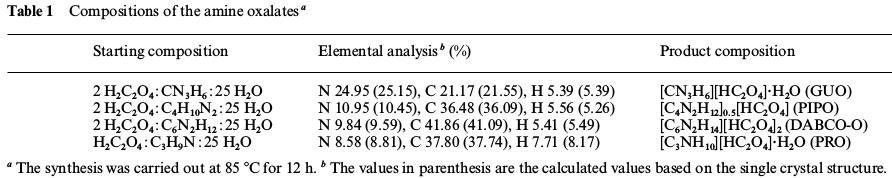
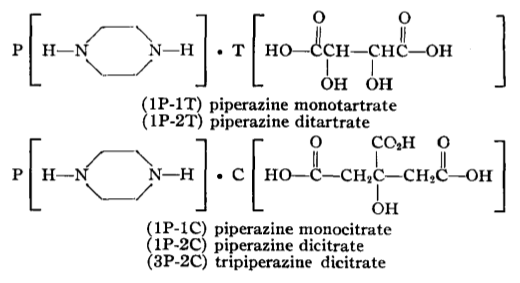
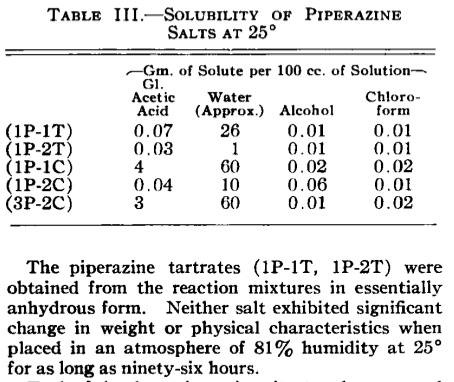

Vzhľad piperazín dioxalátu, ešte vlhký na filtračnom papieri a suchý:


V nasledujúcom experimente sme použili presne 40 gramov piperazín dioxalátu, ako východiskové množstvo pre prípravu podvojného chloristanu. Použili sme meďnatú zlúčeninu pre podvojnú zámenu a vyzrážanie oxalátového aniónu z roztoku. Samozrejme, napríklad hydroxid vápenatý alebo uhličitan by bol lacnejší, no nebolo by vidno farebnú zmenu počas priebehu reakcií, hlavne na konci by sme si neboli istí, či reakcia prebehla dobre, roztok by bol od začiatku do konca biely/bezfarebný (no keďže už vieme, že reakcia prebieha hladko, nabudúce použijeme). Použili sme pomer surovín 1:2:2 pre dioxalát, kyselinu chloristú a CuO, postup nebol optimalizovaný, ale pre fotenie bol vhodný. Do 200 ml vody (trochu málo, ako sme zistili) sme pridali 23,9 gramu CuO a 42,2 gramu koncentrovanej HClO4 a zohriali ju za miešania na horúcom vodnom kúpeli. Polovica oxidu sa rozpustila, vznikla modročierna zmes s roztokom chloristanu:

Do tejto horúcej miešanej suspenzie sme pomaly po malých dávkach pridávali práškový dioxalát piperazínu, zmes bola postupne svetlejšia. Záber nižšie je po pridaní prvej polovice dioxalátu. Ak by sa nezreagovaný CuO tak veľmi rýchlo neusadzoval, suspenzia už aj s oxalátom meďnatým by bola na fotke o niečo tmavšia. Zmes ešte nebola príliš hustá, ľahko stekala zo stien misy.

Dioxalát sme pridávali asi polhodinu, ďalšiu polhodinu sme zmes ešte dodatočne zohrievali a miešali, aby reakcia prebehla kompletne. Zmes zhustla už od všetkého vyzrážaného oxalátu Cu, plus sa samozrejme odparilo niečo vody, očividne sme jej použili málo (ale na spodku zostalo len veľmi málo nezreagovaného oxidu Cu):

Suspenziu oxalátu Cu v roztoku chloristanu piperazínu sme dodatočne zriedili vodou, prefiltrovali, oxalát opäť prevarili s malým množstvom vody a zas filtrovali a myli, a premyli sme samozrejme aj filtračné papiere. Výsledný roztok chloristanu piperazínu bol mierne zelenkastý, nevylučujeme, že mikroskopické množstvo oxalátu medi predsa prešlo, alebo to boli vedľajšie produkty reakcie, aj pre príliš hustú zmes na konci (vieme, že hydrogenoxalát medi existuje, no nenašli sme údaje o jeho rozpustnosti ale nevieme, či náhodou neexistuje aj dáky podvojný oxaláto-chloristan meďnatý alebo podvojný oxalát piperazíno-meďnatý... Chloristan meďnatý nebol v nadbytku) pH roztoku bolo cca 5:


Pokusne sme vodu z časti roztoku chloristanu odparili pomaly, voľne na vzduchu, z inej časti na vriacom vodnom kúpeli - z pomaly, za chladu odpareného roztoku sme získali kryštály dokonale suché, nehygroskopické, no pri odparovaní nad vriacou vodou sa pH roztoku počas procesu zmenilo na cca 2 a získané kryštály boli stále vlhké, neschnúce. Toto je vzorka za horúca získaného surového piperazín perchlorátu:

Na obrázku to až tak nevidno, no mal modrastý nádych. Zistili sme, že chloristan piperazínu (a taktiež hotový perovskit) je dobre rozpustný v acetóne, takže sme ho prečistili rozpustením v horúcom acetóne (v mútnom roztoku boli očividne malé množstvá dvoch nerozpustných zložiek - svetlomodrej a bielej) a prefiltrovaním roztoku. Ten už nebol sfarbený. A presne naopak - v liehu a hlavne v izopropylalkohole je chloristan (a opäť aj hotový perovskit) rozpustný len veľmi málo alebo vôbec, takže ďalšie čistenie produktu bolo prepláchnutie studeným technickým liehom a potom čistým izopropylalkoholom. Výzor chloristanu piperazínu ešte pred preplachovaním (tušíme, že kvôli kryštalizácii z acetónu to asi nebude dihydrát):

Nakoniec, po preplachovaní a vysušení, sa na váhy dostalo cca 39,7 gramu chloristanu. Vo forme jemného bileleho prášku:

Je otázne, koľko vody obsahuje. Ak by bol bezvodý, tak by to bol zisk okolo 92%, a ak dihydrát, čo určite nie je, tak okolo 82%. Nemáme informácie, ako sa dihydrát správa, napr. či zvetráva na vzduchu a naopak, či bezvodý je hygroskopický. Náš produkt sa dá pomerne ľahko zapáliť (nezdá sa, že by sa prv topil) a kľudne deflagruje. No vedľajšie produkty (alebo produkt) reakcie počas jeho prípravy, ktoré zostali na filtračnom papieri po filtrácii acetónového roztoku, sú omnoho ľahšie zápalné a deflagrujú neporovnateľne prudšie. Je pravdepodobné, že sme nechtiac získali látku, ktorá sa asi zatiaľ nikde nespomína. Zatiaľ nie je isté, či energetickou zložkou je tá biela alebo modrá, či obe. Deflagrácia látky produkuje hustý čierny dym a ako sme zistili, sú to sadze. Je možné, že tá látka vziká až v prítomosti acetónu (je jedným z reagentov). Pôvodne sme náš piperazín perchlorát chceli ešte rekryštalizovať z vody, no nakoniec sme sa rozhodli, že k jeho horúcemu koncentrovanému roztoku pridáme priamo roztok chloristanu sodného v pomere ako k bezvodnému chloristanu piperazínu (overili sme si, že to nebol dihydrát - po pridaní malého množstva vody k nemu, vodu rýchlo vsiakol a rýchlo tuhol na tvrdé zlepence), a to tak, že sme použili 1/10 mólu chloristanu piperazínu, čiže cca 28,7 gramu, potom 14,2 gramu koncentrovanej HClO4 a 8,4 g NaHCO3. Na horúcom vodnom kúpeli bol roztok zohrievaný až vznikla hustá kaša, tá bola chvíľu miešaná za chladnutia, potom bol pridaný lieh, miešané bolo až do vychladnutia, filtrované, premyté ešte raz liehom a potom izopropylakoholom. Po vysušení sme získali množstvo cca 32,8 gramu, čo je zisk prakticky 80 percent, ako to je aj spomenuté v papieri. Produkt je suchý, sypký, ťažký mikrokryštalický práškok:

No ešte zaujímavejší experiment nasledoval so zbytkom chloristanu piperazínu: tých cca 11 gramu sme opäť rozpustili v malom množstve horúcej vody a k nemu sme pridali 4,45 (o niečo menej ako teor. množstvo) gramu NH4ClO4, takmer okamžite sa rozpustil a roztok sme podobne zahustili a prepláchli ako predtým. Všetko prebiehalo rovnako, taktiež sa rovnako vylúčila/vyzrážala ťažká sypká, kryštalická látka, bez nejakých nehomogenít (no, keď nepočítame napadaný prach, čo je ale v improvizovaných podmienkach bežné), v množstve 12,6 gramu, by to bol zisk prakticky 82 %, počítané na chloristan amónny:

Vypočítané detonačné parametre tejto zlúčeniny sú zas 8629 m/s, 32,4 GPa pri 1.74 g/cm3, teda ak nepočítame vyššiu hygroskopicitu, tak výhodnejšie je pripravovať sodnú soľ.
A ohľadom rozpustnosti (alebo skôr nerozpustnosti) týchto perovskitov, zdá sa, že je "prikrášľovaná", buď zámerne (samozrejme, robí sa to) alebo zlým prekladom z čínštiny (pozrite napr. tento papier, je realistickejším pohľadom na ich rozpustnosť), prakticky nikde sa v týchto papieroch presne nerozoberá.
Čo sa týka využitia v NPED rozbuškách (to nás zaujíma najviac), hlavne bola doteraz testovaná sodná soľ. V množstve okolo 500 mg je spoľahlivo využiteľná v mosadzných rúrkach/nábojniciach (minimálne detonujúce množstvo od čiernoprachovej šnúry bolo takých 250-350 mg), lepšie v tenších, ako širších samozrejme. No v plastových rúrkach (aj vo viacerých vrstvách) je to zložitejšie, prášok je citlivý na hustotu lisovania a hrúbku/dĺžku náplne, a buď detonuje alebo len kľudne "vyfučí", zatiaľ sme sa s ničím medzi tým nestretli (slabá deflagračná explózia).
Neskôr sme sa pokúsili vyrobiť piperazín diperchlorát metódou chloristan vápenatý/zásaditý uhličitan meďnatý, s miernym nadbytkom týchto zložiek (hlavne uhličitanu), či zisk bude vyšší. Zdá sa, že bol (ale to mohlo byť zapríčinené aj inými faktormi), no produkt bol aj viac znečistený, pravdepodobne roztok piperazín diperchlorátu reagoval s nadbytkom uhličitanu Cu a vznikol zelený rozpustený komplex - po pridaní malého množstva kyseliny chloristej farba roztoku značne vybledla. K pokusom s novou várkou sme sa vrátili, v súvislosti s piperazíno-striebornou soľou, ktorá má sľubované detonačné parametre 8961 m/s, 42,4 GPa pri 2,5 g/cm3 a viac sa blíži traskavinám (viac v tomto papieri). Bola pripravená priamou reakciou horúceho vodného roztoku chloristanu Ag (ten bol pripravený zohrievaním roztoku dusičnanu Ag s kyselinou chloristou) s chloristanom piperazínu, voda bola odparená a produkt 3-krát postupne prepláchnutý liehom. Pracovali sme s množstvom 1/50 mólu, po každom prepláchnutí niekoľkými mililitrami liehu sa niečo látky rozpustilo a hmotnosť produktu po každom vysušení vždy klesla o necelý gram, teda rozpúšťa sa aj v liehu pomerne dobre. Aj po trojnásobnom prepláchnutí biely kryštalický prášok vytvára dojem, akoby bol vždy mierne vlhký (už po prvom prepláchnutí a vysušení sa vlastnosti nemenili, čiže nespôsobuje to rozpustná prímes), nie je to celkom taký sypký prášok ako v prípade Na a NH4 perovskitov, teda buď je látka aj samotná mierne hygroskopická, alebo je to naozaj len iná kryštalická štruktúra (látka nevytvára na papieri vlhké stopy, len sa sype v takých "zlepencoch"). Asi skôr to druhé, lebo skúšali sme látku ponechať niekoľko hodín v suchu, potom rovnaký čas v prírodnom vlhku a aj v zaparenej miestnosti - zdá sa, že sa mechanické vlastnosti nemenia, alebo len nepatrne, sypkosť je podobná, absolútne nenastáva žiadne "sirupizovanie", ako by možno niekto čakal, že kvôli obsahu chloristanu Ag sa tak látka bude správať. Malá štipka látky od kontaktu s plameňom okamžite deflagruje, podobne ako zábleskový prach, ale bez toho oneskorenia a prudšie ako pri ostatných dvoch perovskitoch (teda, ak je tam teoreticky aj trochu vody, vždy sa látka správa energickejšie). Hmotnosť zlúčeniny sa po prepláchnutí už státím na vzduchu nemení, zdá sa. Nakoniec sme získali cca 81% produktu (z toho asi 5% aj z toho preplachovacieho liehu po ochladení a čiastočnom odparení a táto časť mala rovnaké vlastnosti ako zvyšok, teda nedeje sa tam žiadne vymývanie chloristanu Ag, tie dva chloristany držia spolu dobre). Je otázne, ak aj chloristan striebra aj piperazínu tvoria hydráty, či aj podvojná soľ nie je hydrát. Soľ je patentovaná, no patent ešte počas našich pokusov nebol k dispozícii, v ňom by mali byť podrobnosti, dúfame. Látka aj opticky vytvára dojem "kyprosti", pričom je stále dostatočne ťažká:

Spravili sme testy prechodu z deflagrácie do detonácia v niekoľkých vrstvách alobalu, papierových rúrkach obalených gumovou páskou a taktiež v plastových rúrkach (v kovových hrubostenných nás to nezaujíma, pre obsah striebra - chápete, ak iné strebro obsahujúce traskaviny detonujú bez takéhoto obalu, načo by nám to bolo). Už testy v alobale vyvolali sklamanie, keďže 40-180 mg množstvá len deflagrovali, v papierovej rúrke už ale cca 220 mg naznačovalo čiastočnú detonáciu. V plastove rúrke išlo tiež všetko hladko v nelisovanom stave, no jedna lisovaná náplň, cca 640 mg, len kľudne a značne pomaly vyhorela, čo sa nám už stalo aj pri ostatných perovskitoch - to bolo nepochybne spôsobené málo pórovitou časťou pri zápalnici, kde sa DDT rozbehne, no pravdepodobne v kombinácii s rozšíreným/vypáleným otvorom na rúrke od horiacej zápalnice, kade tlak prudko unikol (hádame to z toho, že nie vždy sa nám to s lisovanými perovskitmi stáva). Teda táto látka nie je v porovnaní napr. s azidom alebo nitrotetrazolátom Ag vôbec výhodná (ako traskavina samozrejme - občas nastávajú nedorozumenia, keď testujeme látku ako traskavinu, teda aké malé množstvo, nelisované i lisované, detonuje od tepla v rôznych obaloch, kým zopár ľudí si hlúpo myslí, že testujeme jej výkon - mnohí sú už skutočne zmagorení túžbou po výkone a dokonalosti, a nie len raz), ak nepočítame azda jej ľahšiu výrobu a vyššiu bezpečnosť, no je ľahko rozpustná a teoreticky len o málo výkonnejšia ako sodná soľ, tá ju odstrkáva bokom ak by sme ju cheli použiť ako sekundárnu náplň, no pravdepodobne strieborná soľ má ešte nižší kritický priemer a bezpochýb neporovnateľne ľahšiu iniciovateľnosť, čo ju možno predurčuje na použitie v mikrorozbuškách (napr s priemerom a dĺžkou len niekoľko mm), v kombinácii s priam mikroskopickým množstvom vysokoúčinnej traskaviny, napr. nitrotetrazolátom striebra, čo nás dosť zaujíma. My túto látku (zatiaľ) nepodceňujeme, len ako traskavina sa nám ukázala byť neekonomická a neefektívna (aby nedošlo k nedorozumeniam pri budúcich testoch a videách). Teda preto sme testovali miniatúrne rozbušky, zatiaľ ich spoľahlivosť a brizanciu na plechovkách, s vnútorným priemerom menej ako 1,5 mm (použitá rúrka bola medicínska vnútrožilná). Ag perovskit fungoval skvele pri takomto priemere, vykazoval vysokú brizanciu, veľmi porovnateľnú s čistým nitrotetrazolátom Ag. Náplne sme nevážili, pri nepresnosti váhy ktorú práve používame to nemalo zmysel a lisovali sme len mierne (pre citlivý nitrotetrazolát a mäkkosť rozbušiek) tenkým drievkom. Látky vlastne boli porovnávané skôr objemovo. Testovali sme ešte o niečo menšie verzie na pentrite aj chloristane pyridínu, vyvolali detonáciu, preto budeme tieto rozbušky ďalej miniaturizovať, plus budeme testovať aj ich elektrické verzie (v poslednej dobe sme sa dosť zaoberali nezvyčajnými "diaľkovými spínačmi", aké asi nikto iný nepoužíva, totiž bežné riešenia nás nezaujímajú. Zverejníme len naozaj tie "najnevinnejšie" riešenia, ako vždy).
Zaujímala nás aj svetelná stabilita striebornej soli, preto sme dve vzorky ponechali na svetle jeden mesiac (v lesnom prostredí, zakryté priehľadným obalom), neprepláchnutú a prepláchnutú liehom, aký bude medzi nimi rozdiel. Už skoro bolo vidno, že neprepláchnutá získava špinavú farbu a hlavne vzlínavosťou v prítomnosti vlhka sa na stenách nádoby začal vytvárať tmavý strieborný povlak, kým ľahko prepláchnutá soľ je na tom oveľa lepšie - aj tu bolo vidno, že kým vzorka stmavla len nepatrne, opäť vzlínavosťou sa na stene nádoby vytvorilo čosi tmavého povlaku, teda to vyzerá tak, že samotná látka na svetlo nereaguje vôbec alebo len nepatrne, kým tmavnutie spôsobuje neželaná, zle vymytá prímes, pravdepodobne nadbytok prekurzoru alebo vedľajší produkt (samozrejme, pre pripomenutie, nadmerné umývanie produktu liehom zas znižuje zisk). Prvý obrázok je vzorka neprepláchnutá, druhá už áno:


Pokračovanie...


