Nitrotetrazoláty
V tomto príspevku budú v rôznych časových odstupoch (ako to autor uzná za vhodné) popísané niektoré, menej či viac známe soli nitrotetrazolu (hoci aj menej výkonné, zato však bezpečnejšie). Zopár nitrotetrazolátov je už podrobne popísaných na rôznych webových stránkach alebo vo voľne dostupných dokumentoch (napr. nitrotetrazolát meďný - DBX-1, strieborný, ortutnatý, niektoré podvojné soli a komplexy), takže tieto, ak tu budú spomínané, tak len ich menej známe vlastnosti.
Najprv by asi bolo vhodné spomenúť obyčajný nitrotetrazolát meďnatý (Cu(CN5O2)2.xH2O), keďže informácií o ňom je málo (ani Bagal, Bubnov a Fedoroff neposkytujú spoľahlivé informácie - býva zamieňaný s kyslou meďnatou soľou a informácie sú často nepresné) a mnohých by iste zaujímal kvôli jednoduchosti výroby a cene (ak by mal použiteľné vlastnosti) alebo jednoducho len preto, prečo sa neujal ako traskavina.
Zdá sa, že už bol testovaný ako náhrada azidu olovnatého v iniciátoroch, pričom pri optimálnom lisovacom tlaku bezvodý nitrotetrazolát výkonom až tak veľmi nezaostával za azidom (pozri dokumenty 1, 2) a bol na počudovanie považovaný za kvalitnú traskavinu, ako aj tvrdí toto zhrnutie (dokument Environmentally Friendly Energetic Materials for Initiation Devices):

Hydrát bol "eliminovaný" ako náhrada azidu Pb (mohol to byť problém so štruktúrou kryštálov, Bagal však tvrdí, že nedisponuje iniciačnou schopnosťou, čo však nie je pravda. Spomína tetrahydrát - ak píše o kyslej soli, tak tá je ešte značne explozívnejšia ako normálna - nepatrný suchý povlak kyslej soli na filtračnom papieri je po zapálení schopný veľmi silno explodovať, povlak normálnej soli reaguje značne miernejšie):

Reakciou vodných roztokov nitrotetrazolátu sodného a síranu meďnatého pri izbovej teplote vzniká Cu(NT)2 vo forme objemnej modrej zrazeniny, ktorá po vysušení tvorí kyprý svetlomodrý prášok (v literatúre sa očividne často zamieňa s kyslou soľou Cu(CN5O2)2.CHN5O2.4H2O, ktorá má ale hráškovozelenú farbu) alebo zlepence s nízkou hustotou (už toto je dosť negatívna vlastnosť zlúčeniny), na dotyk takmer pripomína mastenec alebo púder - to je jednoznačne nepríjemná forma pri manipulácii. V horúcej vode je veľmi dobre rozpustný, v studenej značne menej, ale dosť na to, aby viacnásobným prepláchnutím zrazeniny sa jej objem viditeľne zmenšil (voda odtekajúca z filtra mala vždy rovnaký odtieň modrej farby). Soľ vykryštalizovaná z vody je pravdepodobne dihydrát a zatiaľ nebolo skúšané dehydrovať ju v improvizovaných podmienkach. Je málo citlivá na trenie (trecia miska alebo kameň/kameň - nepodarilo sa vyvolať explóziu, no nárazmi explodovala - bezvodá je podľa údajov na trenie citlivá takmer ako styfnát Pb, čo ani to nie je príliš vysoká citlivosť) a pri kontakte s plameňom nastávajú len miestne detonácie alebo deflagrácie, pri pomalom zohrievaní sú explózie značne silnejšie (strata hydrátovej vody). Zabalená v hliníkovej fólii od horiacej zápalnice viacero krát silno exploduje so zábleskami a časť soli je rozmetaná, no s rovnakým obalom vhodená do ohňa však detonuje kompletne a silno.
Zaujímavé je, že citlivosť nitrotetrazolátu je závislá od spôsobu prípravy (iný tvar kryštálov?):
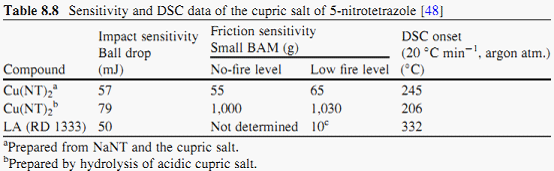
Spôsob prípravy vplýva takisto aj na explozívnosť zlúčeniny:

Vzhľad suchého hydrátu nitrotetrazolátu meďnatého (dihydrát?):

Zbytky nábojnice po teste iniciačnej účinnosti hydrátu nitrotetrazolátu Cu, teda Bagal nemá pravdu (nitrotetrazolát, 0,06 gramu, bol len mierne lisovaný, pentrit bol lisovaný):

Hydrát sa určite nedá porovnať s azidom Pb, ale jednoznačne má iniciačnú schopnosť a jeho nízka citlivosť na trenie z neho robia zaujímavú, lacnú a jednoduchú traskavinu (kvalitou však určite zaostáva za jeho podvojnými soľami s nitrotetrazolátom sodným alebo amónnym, výhodná je však jeho nižšia cena). Táto látka sa taktiež ukázala byť vhodnou formou na dlhodobé bezpečné skladovanie nitrotetrazolového aniónu. Po takmer ôsmich rokoch skladovania nenastala žiadna zmena a soľ sa dala hneď použiť napr. na prípravu nitrotetrazolátu Ag.
Vo videu nižšie vidno nepredvídateľnú reakciu nepatrného množstva hydrátu Cu(NT)2 na plameň zápalky. Pri prvom pokuse o iniciáciu zlúčenina pravdepodobne zahriatím stratila malú časť svojej hydrátovej vody, pretože pri druhom pokuse už explodovala kompletne.
Pokračovanie...


